Gestion des risques selon la norme DIN EN ISO 14971
La sécurité des patients, des médecins et des infirmières est d’une grande importance pour Interelectronix . En introduisant un système de gestion des risques pour les dispositifs médicaux conformément à la norme DIN EN ISO 14971, nous sommes plus qu’à la hauteur de notre maxime.
Quelles que soient les réglementations légales, l’application de la gestion des risques de l’idée du produit à la mise sur le marché est pratiquée de manière cohérente à Interelectronix dans tous les processus et départements et comprend les composants suivants:
-Analyse du risque -Évaluation du risque
- Contrôle des risques
- Analyse des informations relatives aux risques provenant de l’observation du marché
- Évaluation des enseignements tirés du processus de gestion des risques
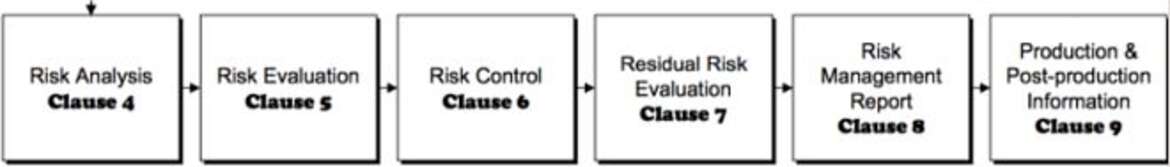
Si nécessaire, un ajustement dynamique de la gestion des risques pour les dispositifs médicaux est effectué grâce à une observation étroite des produits et de leurs fonctions en cours d’utilisation, en tenant compte des types de dangers respectifs.
Les produits de technologie médicale doivent être à la fois sûrs et efficaces à utiliser. Par conséquent, il est logique d’appliquer la gestion des risques dès la phase de développement.
L’objectif premier de Interelectronix gestion des risques est donc d’assurer l’élimination ou la minimisation des risques par des mesures conceptuelles ou constructives.
Cela commence par la conception d’un produit et s’étend à tous les processus, procédures et procédures de production.
L’analyse des risques est un élément important de la gestion des risques
La réalisation d’une analyse des risques est requise par les procédures d’approbation dans l’UE et par la FDA. C’est un moyen efficace d’orienter les efforts de développement et de validation de produits là où les risques les plus importants peuvent survenir.
L’analyse des modes de défaillance et de leurs effets (AMDEC) a jusqu’à présent été un élément essentiel de l’assurance qualité avant le début de la production en série. Cependant, les analyses de risques selon la norme DIN EN ISO 14971 diffèrent considérablement de celles de l’AMDEC.
L’analyse des modes de défaillance et des effets n’est donc plus reconnue par les organismes d’homologation pour l’homologation des dispositifs conformément à la norme EN 60601-1 3e édition.
MOPP - Moyens de protection des patients
La norme CEI 60601-1 définit les « moyens de protection du patient (MOPP) pour réduire le risque de choc électrique pour le patient ».
En conséquence, les dispositifs médicaux doivent toujours être équipés de deux mesures de protection indépendantes pour la protection des patients afin d’être « les premiers à l’épreuve des défauts ».
Si l’une des deux mesures de protection échoue, la sécurité du patient ne doit pas être compromise. Selon le type de danger, plusieurs systèmes de protection travaillent généralement côte à côte, qui sont destinés à contrer différents potentiels de danger.
-Résistance diélectriqueUne résistance diélectrique élevée est destinée à protéger contre les surtensions pulsées qui se produisent fréquemment dans les systèmes électriques.
Structure isolante spécifique à l’applicationUne structure isolante spécifique à l’application est destinée à prévenir le risque d’isolation inadéquate en raison de défauts de fabrication ou du processus de vieillissement.
Distances de dégagement et de fuiteLes environnements humides ou poussiéreux peuvent entraîner des embrasements électriques, qui doivent être évités au moyen de distances de dégagement et de fuite.
Courants de fuite - courants de fuiteLes patients doivent être protégés contre les courants de fuite en les réduisant aux valeurs maximales des courants de fuite (la norme dépend de l’appareil).
Raccords conducteurs de protectionLes raccords de conducteurs de protection sont conçus pour dissiper les courants dangereux afin qu’ils n’atteignent pas le patient.
Courant de fuite patient (DIN 60479-1)Le courant de fuite du patient est créé par un circuit électrique défectueux dans l’appareil, qui circule soit directement via le conducteur de protection, soit indirectement sous forme de courant de fuite de dispositif via des pièces conductrices du dispositif vers la terre, ce qui présente un danger pour les patients.
Systèmes tactiles et IHM selon la norme IEC/UL 60601-1
En particulier dans la technologie médicale, la sécurité des appareils, la protection individuelle, une hygiène élevée, une longue durée de vie, la fiabilité et une intégration fonctionnelle efficace sont de la plus haute importance. Tous les écrans tactiles et systèmes tactiles développés par Interelectronix sont soumis aux exigences de sécurité élevées pour les dispositifs médicaux conformément à la norme de base IEC/UL 60601-1.
La norme IEC/UL 60601-1 définit les exigences générales relatives aux caractéristiques de sécurité de base et de performance essentielles des systèmes électromédicaux connectés à un réseau d’alimentation destinés au diagnostic, au traitement ou à la surveillance d’un patient. La norme européenne EN 60601-1 est identique à la norme IEC/UL 60601-1.
En raison de leur grande fiabilité et de leur technologie de pointe, de leur conception innovante et de leur facilité d’utilisation intuitive, les systèmes tactiles Interlecronix sont utilisés par
- Appareils à ultrasons
- Appareils à rayons X
- Scanners de tomodensitométrie
- Matériel d’analyse de laboratoire
ainsi que
- en salle d’opération
- en médecine dentaire
- dans le suivi des patients
- et l’enregistrement des patients
utilisé.
Dans le cas des écrans tactiles utilisés dans la technologie médicale, le courant de fuite du patient peut être évité soit par une conception spécifique, une isolation ou l’utilisation de matériaux appropriés tels que des boîtiers en plastique ou des panneaux frontaux.
Chaque écran tactile utilisé dans la technologie médicale est soumis à un contrôle précis du flux de courant exact pour détecter et éviter le courant de fuite de l’appareil.
Tests de protection selon IPX1 à IPX8
Les écrans tactiles des dispositifs médicaux sont soumis à des exigences de sécurité particulièrement élevées. Par exemple, les systèmes tactiles doivent souvent fonctionner sans erreur pendant des années dans des conditions difficiles tout en assurant une protection complète des patients et du personnel opératoire.
Les écrans tactiles utilisés dans la technologie médicale sont soumis à une exposition considérable aux agents de nettoyage, aux désinfectants, à l’eau, aux vapeurs, aux acides ou aux fluides corporels. De plus, la pénétration de corps étrangers et de poussières, ainsi que la contamination par des bactéries et des virus, doivent être pratiquement éliminées.
En fonction des exigences et des domaines d’application respectifs, Interelectronix développe des systèmes tactiles prêts à installer qui répondent aux différentes classes et normes de protection d’IPX1 à IPX8 :
- Protection contre les corps étrangers (DIN 40 050 Partie 9 ou DIN EN 60529)
- Protection contre l’eau (DIN 40 050 Partie 9 ou DIN EN 60529, tests de classe de protection de l’eau)
- Résistance aux chocs (DIN EN 62262)
En tant que spécialiste des systèmes tactiles de haute qualité et prêts à installer, Interelectronix possède de nombreuses années d’expérience dans le développement d’écrans tactiles, d’écrans tactiles et de systèmes tactiles complets qui répondent aux exigences particulières de la technologie médicale en matière de sécurité, de durabilité et de protection des patients.
Une large gamme de verres, de matériaux de boîtier, de joints de haute qualité et de techniques de laminage permet la construction d’IHM (interface homme-machine) conforme IPX1 à IPX8.